
Guia de Interpretação do VENTANA
MMR RxDx Panel para o Carcinoma do
Endométrio (CE)
VENTANA anti-MLH1 (M1) Mouse Monoclonal Primary Antibody
VENTANA anti-PMS2 (A16-4) Mouse Monoclonal Primary Antibody
VENTANA anti-MSH2 (G219-1129) Mouse Monoclonal Primary Antibody
VENTANA anti-MSH6 (SP93) Rabbit Monoclonal Primary Antibody


Índice
Introdução 1
Utilização pretendida 3
Aplicação do produto 3
Objetivo do guia de interpretação 3
Avaliação clínica 4
Caraterísticas de coloração 4
Critérios de aceitabilidade da morfologia e da coloração de fundo 5
Critérios de caso da avaliação clínica 5
Algoritmo de pontuação 6
Controlos 8
Controlos positivos internos 8
Fluxo de trabalho de amostras 10
Imagens de referência 12
Casos proficientes 12
Casos deficientes 14
Casos desafiantes 18
Impacto das condições pré-analíticas no VENTANA MMR RxDx Panel 28
Condições de fixação aceitáveis para obter resultados de coloração ótimos 28
Estabilidade das lâminas de corte 32
Espessura do tecido 32
Referências 33


A reparação de erros de emparelhamento do DNA (MMR) é um
mecanismo de conservação molecular que serve para corrigir
substituições incorretas de bases que ocorrem espontaneamente
durante a replicação do DNA. Os métodos baseados na
reação em cadeia da polimerase (PCR) demonstraram que
falhas na MMR dão frequentemente origem a instabilidade
de microssatélites (MSI), uma condição em que repetições
curtas e em tandem de nucleótidos são inseridas no DNA.
Quando o número de repetições é igual ou superior a 30% dos
loci de microssatélites examinados, a MSI pode ser também
caracterizada como MSI-High (MSI-H). Estes defeitos nos
mecanismos de MMR foram atribuídos a mutações nas proteínas
de MMR, mais comummente na MLH1, PMS2, MSH2 e MSH6.
As proteínas MLH1 e PMS2 normalmente funcionam em
conjunto num complexo heterodimérico, tal como acontece com
as proteínas MSH2 e MSH6. Quando a MMR está a funcionar
normalmente, o heterodímero MSH6/MSH2 liga-se ao DNA
que contém erros de emparelhamento. Esta ligação induz uma
alteração conformacional que permite que o heterodímero MLH1/
PMS2 se ligue ao complexo MSH6/MSH2 ligado ao DNA, o que
resulta na reparação por excisão do DNA afetado. Mutações ou
deficiências nestas proteínas têm frequentemente como resultado
a MSI e mutações somáticas causadas por erros de replicação.
É possível demonstrar que os testes imuno-histoquímicos
(IHC) de MMR são úteis na identificação dos genes de MMR
com probabilidades de conter alterações de linha germinal ou
somáticas.
Tradicionalmente, os regimes de tratamento dos pacientes
oncológicos têm sido ditados especificamente pela doença maligna
em questão. No entanto, as imunoterapias que estão a surgir,
particularmente aquelas que modificam as vias celulares das
proteínas de morte programada 1 (PD-1) ou do ligando de morte
programada 1 (PD-L1), estão a permitir reformular as estratégias
terapêuticas utilizadas pelos médicos. A PD-1 é um recetor com
função inibidora que é expresso nas células T após a ativação das
células T, mantendo níveis sustentados em estados de estimulação
crónica, como as infeções crónicas ou o cancro. A expressão
da PD-L1 tem sido observada em células imunitárias e células
malignas, tendo sido reportado que a expressão aberrante da
PD-L1 nas células tumorais (TC) impede a imunidade antitumoral,
resultando em evasão imunitária. Por conseguinte, a interrupção
da via da PD-L1/PD-1 representa uma estratégia atraente de
revigoração da imunidade das célulasT específicas de tumores.
As proteínas de MMR (MLH1, PMS2, MSH2 e MSH6) encontram-
se expressas em células normais proliferativas e em células
malignas ubiquamente. Muitos dos cancros mais comuns têm
deficiências na MMR (dMMR) e apresentam MSI. Vários estudos
demonstraram que a deficiência na MMR está correlacionada
com uma expressão mais elevada das proteínas PD-1 ou
PD-L1. Assim, as proteínas de MMR podem ser úteis como
biomarcadores preditivos para a terapêutica direcionada para
a PD-1; mais especificamente, a perda de expressão de uma ou
mais proteínas de MMR pode ajudar a prever uma probabilidade
acrescida de resposta a este tipo de terapêutica. Os inibidores
da PD-1 podem ser benéficos em muitos cancros comuns
com frequência elevada de deficiência na MMR e/ou MSI-H,
independentemente do tecido de origem do cancro. Logo, os
pacientes para os quais estiver a ser considerada a terapêutica
direcionada para a PD-1 irão beneficiar de um ensaio de
diagnóstico complementar a fim de identificar a população de
pacientes que apresenta deficiência na MMR.
O carcinoma do endométrio (CE) é uma das doenças malignas
ginecológicas mais comuns.
12
Observam-se frequentemente
nesta patologia muitas alterações genéticas, nomeadamente
MSI.
12
Foi também sugerido que o CE com MSI pode apresentar
expressão aumentada da proteína PD-L1, em comparação com
o CE com estabilidade de microssatélites (MSS).
16
Apesar de o
tratamento do CE variar em função do grau, histologia e estádio
da doença,
17
a avaliação do estado da MMR nos tumores de CE
é útil em termos de prognóstico e de orientação do tratamento
12
.
Consequentemente, as pacientes para quem está a ser
considerada terapêutica direcionada para a PD-1 irão beneficiar
de um ensaio de diagnóstico complementar para identificar o seu
estado de MMR.
A perda de expressão de qualquer uma das proteínas de MMR
essenciais, nomeadamente da MLH1, da PMS2, da MSH2 ou da
MSH6, provoca deficiência na MMR. A presença de coloração nos
quatro marcadores de proteínas de MMR no tumor indica que o
caso é proficiente no que diz respeito ao estado VENTANA MMR
IHC. A ausência de coloração em qualquer dos marcadores de
proteína de MMR do VENTANA MMR RxDx Panel indica que o caso
é deficiente no que diz respeito ao estado VENTANA MMR IHC.
Introdução
VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 1

2 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio

Utilização pretendida
Aplicação do produto
Consulte os folhetos informativos de VENTANA MMR RxDx
Panel para mais informações sobre a utilização pretendida deste
produto, incluindo indicações associadas.
Objetivo do guia de interpretação
Este guia destina-se a:
• Fornecer aos patologistas uma ferramenta para facilitar
a avaliação clínica de secções de tecido de tumor fixadas
em formol e impregnadas em parafina (FFPE) coradas com
VENTANA MMR RxDx Panel, de acordo com a rotulagem do
produto proposto.
• Fornecer imagens fotográficas para ilustrar os padrões
de coloração que podem resultar da coloração de tecidos
tumorais com o VENTANA MMR RxDx Panel.
• Fornecer imagens exemplificativas de amostras desafiantes
para oferecer orientação na sua avaliação.
• Fornecer orientações para a utilização de elementos de
tecido normal positivo para as proteínas de MMR que sirvam
de controlo interno positivo quando corados com VENTANA
MMR RxDx Panel.
VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 3

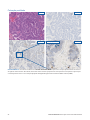
Estado de coloração Intacto e de Perda de MMR: nestes casos de carcinoma do endométrio, os núcleos apresentam coloração
inequívoca, que é o padrão de coloração predominante observável na maioria dos tecidos tumorais no Estado Intacto de MSH6
(painel da esquerda). A ausência de qualquer coloração nuclear em tecidos tumorais representa Estado de Perda de MSH6 (painel
da direita). A coloração nuclear inequívoca em células de controlo interno (i.e., linfócitos) nas proximidades de tumores viáveis serve de
controlo positivo interno aceitável.
Caraterísticas de coloração
Avaliação clínica
As células marcadas com cada ensaio no VENTANA MMR RxDx
Panel são avaliadas quanto à presença ou ausência do sinal
diaminobenzidina (DAB). A coloração com o VENTANA MMR
RxDx Panel em proteínas de MMR segue um padrão nuclear. A
perda de qualquer uma das proteínas de MMR detetadas pelo
VENTANA MMR RxDx Panel é observada nos núcleos das células
tumorais. O estado de MMR é classificado como intacto ou perda
apenas com base numa coloração nuclear inequívoca.
• O Estado Intacto é caracterizado por células tumorais que
apresentam uma coloração inequívoca de intensidade igual ou
superior à dos controlos internos acima da coloração de fundo.
• O Estado de perda é caracterizado pela ausência de
qualquer sinal detetável. Os casos de perda podem continuar a
apresentar descoloração nuclear cinzenta-pálida.
O sinal pode estar distribuído homogeneamente, com um nível
uniforme de intensidade nas porções neoplásicas do tumor, ou
estar distribuído heterogeneamente, com mais do que um nível
de intensidade. Deve ser facilmente detetável em ampliações de
baixa potência, como 2x ou 4x. É fornecida uma representação
gráfica de tipo(s) de células neoplásicas/elementos de coloração
marcados com VENTANA MMR RxDx Panel na secção Imagens
de referência deste guia de interpretação. O controlo de
reagente negativo (NRC) com correspondência de espécie é
utilizado para avaliar a presença da coloração de fundo nas
amostras de teste e estabelecer uma referência de intensidade
da coloração. Os critérios de aceitabilidade da morfologia e da
coloração de fundo são fornecidos na Tabela 1. Os critérios de
caso para a avaliação do estado de MMR no tecido neoplásico
com qualquer dos quatro ensaios do VENTANA MMR RxDx Panel
são fornecidos na Tabela 2.
Ausência de coloração
nuclear em células tumorais
Coloração nuclear inequívoca
em células tumorais
Coloração nuclear forte
em linfócitos
4 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio
MSH6 10x MSH6 10x

Critérios de aceitabilidade da morfologia e da coloração de fundo
Para cada caso corado com VENTANA MMR RxDx Panel, a aceitabilidade da morfologia e da coloração de fundo do tecido são avaliadas
utilizando os critérios descritos na Tabela 1.
Critérios de caso da avaliação clínica
A Tabela 2 apresenta de forma resumida os critérios necessários para uma lâmina com tecido neoplásico ser avaliada em termos do
estado de MMR com qualquer um dos ensaios do VENTANA MMR RxDx Panel.
Critérios Aceitável Inaceitável
Morfologia São visualizados os elementos celulares de
interesse, o que permite a interpretação
clínica da coloração específica
Não são visualizados os elementos celulares de
interesse, o que compromete a interpretação clínica
da coloração específica
Coloração de
fundo
A coloração de fundo não interfere com a
interpretação clínica da coloração específica
A coloração de fundo interfere com a capacidade de
interpretar a coloração específica
Tabela 1: critérios de aceitabilidade da morfologia e da coloração de fundo
Interpretação clínica Critérios do padrão de coloração
Avaliáveis (têm de ser todos verdadeiros)
1. H&E ≥ 50 células tumorais viáveis
2. A lâmina de Negative Reagent Control é aceitável
3. A morfologia é aceitável
4. A coloração de fundo é aceitável
5. Os controlos positivos internos apresentam coloração nuclear inequívoca
Não avaliáveis (se um dos critérios desta
secção for verdadeiro, a coloração da
lâmina deve ser repetida ou o caso deve
ser rejeitado, conforme for aplicável)
1. H&E < 50 células tumorais viáveis
2. A lâmina de Negative Reagent Control é inaceitável
3. A morfologia é inaceitável
4. A coloração de fundo é inaceitável
5. Os controlos positivos internos não apresentam coloração nuclear
inequívoca
6. A interpretação não é possível devido a perda de tecido, ausência de
tumor, artefactos e/ou artefactos de bordos
Tabela 2: critérios avaliáveis e não avaliáveis
VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 5

O VENTANA MMR RxDx Panel inclui quatro ensaios: VENTANA
anti-MLH1 (M1) Mouse Monoclonal Primary Antibody, VENTANA
anti-PMS2 (A16-4) Mouse Monoclonal Primary Antibody,
VENTANA anti-MSH2 (G219-1129) Mouse Monoclonal Primary
Antibody e VENTANA anti-MSH6 (SP93) Rabbit Monoclonal
Primary Antibody. É necessária uma secção de tecido em série
da amostra de teste para a coloração com cada um destes
anticorpos; são necessárias mais secções de tecido em série da
amostra de teste para a coloração com hematoxilina e eosina
(H&E) e com o anticorpo de NRC, correspondente à espécie do
respetivo anticorpo do VENTANA MMR RxDx Panel (Negative
Control (Monoclonal) (mNRC) ou Rabbit Monoclonal Negative
Control Ig (rNRC)).
As células neoplásicas coradas com VENTANA MMR RxDx Panel
são avaliadas quanto à presença ou ausência do sinal de DAB. A
lâmina corada de NRC correspondente é utilizada para avaliar a
coloração de fundo não específica e o grau de coloração de fundo,
que se sabe ocorrer devido a elementos específicos do tecido
(consulte as imagens de casos proficientes e deficientes).
Se a avaliação por H&E indicar que a amostra de paciente é
inadequada (por exemplo, se estiverem presentes menos de 50
células tumorais viáveis), deverá ser obtida uma nova amostra.
A repetição da coloração de uma amostra de um ensaio de
MMR RxDx específico dentro do painel (por exemplo, VENTANA
anti-MLH1 (M1) Mouse Monoclonal Primary Antibody) deve ser
realizada em lâminas não coradas se (1) a lâmina do caso corada
com o NRC apropriado para esse ensaio não apresentar coloração
aceitável, ou (2) se a lâmina do caso corada com esse ensaio
de MMR RxDx específico (por exemplo, VENTANA anti-MLH1
(M1) Mouse Monoclonal Primary Antibody) não for avaliável. Se
qualquer uma das lâminas não for interpretável devido a falta de
coloração nas células do controlo positivo interno, a presença de
artefactos, efeitos de bordos, necrose, falta de tecido ou qualquer
outra razão, a lâmina não pode ser avaliada. Se a coloração de
controlo for aceitável e as lâminas coradas com VENTANA MMR
RxDx Panel forem avaliáveis, as lâminas podem ser avaliadas por
um patologista com a devida formação, tal como é descrito no
Algoritmo de pontuação.
NOTA: o OptiView DAB IHC Detection Kit e o OptiView
Amplification Kit são os únicos reagentes de deteção
recomendados para utilização com o VENTANA MMR RxDx Panel.
As interpretações da expressão proteica e do Estado de MMR do
VENTANA MMR RxDx Panel são fornecidas abaixo nas Tabelas 3
e 4. Os casos representativos são abordados na secção Imagens
de referência.
Avaliação do VENTANA MMR RxDx Panel:
Algoritmo de pontuação
Tabela 4: interpretação do Estado de MMR do VENTANA MMR RxDx Panel
Proficiente Deficiente
As quatro proteínas (MLH1, PMS2, MSH2 e MSH6) do
painel apresentam todas expressão intacta
Pelo menos uma proteína (MLH1, PMS2, MSH2 ou MSH6) do
painel apresenta expressão intacta
Tabela 3: interpretação da expressão proteica do VENTANA MMR RxDx Panel
Expressão proteica intacta Perda na expressão proteica
Coloração nuclear inequívoca em células tumorais
viáveis na presença de controlos positivos internos
aceitáveis (por exemplo, coloração nuclear em
linfócitos, fibroblastos ou epitélio normal nas
proximidades do tumor)
Perda inequívoca de coloração nuclear ou coloração nuclear
focal fraca equívoca nas células tumorais viáveis, na presença
de controlos positivos internos aceitáveis. A coloração nuclear
pontilhada é considerada negativa
6 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio

Diagnóstico clínico de carcinoma do endométrio proficiente
Estado Intacto de MSH2: coloração
nuclear forte na presença de controlos
positivos internos aceitáveis
Estado Intacto de PMS2: coloração
nuclear forte na presença de controlos
positivos internos aceitáveis
Estado Intacto de MLH1: coloração
nuclear forte na presença de controlos
positivos internos aceitáveis
Diagnóstico clínico de carcinoma do endométrio deficiente
Estado de Perda de MLH1: ausência
de coloração nuclear na presença de
controlos positivos internos aceitáveis
Estado de Perda de MSH6: ausência
de coloração nuclear na presença de
controlos positivos internos aceitáveis
Estado de Perda de MSH2: ausência
de coloração nuclear na presença de
controlos positivos internos aceitáveis
MLH1 20x MSH6 20x MSH2 20x
MSH2 20x
PMS2 20x
MLH1 20x
Núcleos
MSH2
positivos
Núcleos
PMS2
positivos
Núcleos
MLH1
positivos
VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 7

Controlos
Quando corados com VENTANA MMR RxDx Panel, os elementos
de tecido normais, como os linfócitos, os fibroblastos ou o epitélio
normal nas proximidades do tumor, apresentam coloração nuclear
das proteínas de MMR. Estes elementos de tecido funcionam como
controlos positivos internos e devem ser aceitáveis para avaliar a
lâmina corada em cada ensaio do painel. Os controlos internos
devem ser avaliados para cada ensaio e devem cumprir os critérios
de coloração para uma interpretação do painel de estado de MMR.
Em caso de ausência de coloração nuclear inequívoca nos linfócitos,
fibroblastos ou epitélio normal nas proximidades do tumor, a lâmina
corada do ensaio deve ser considerada “não avaliável”.
A Tabela 5 descreve os critérios de uma coloração de controlo
interno aceitável.
Avaliável Não avaliável
Presença de coloração nuclear inequívoca em elementos
de tecido normais (por exemplo, linfócitos, fibroblastos ou
epitélio normal) nas proximidades do tumor
Ausência de coloração nuclear inequívoca em elementos de
tecido normais (por exemplo, linfócitos, fibroblastos ou epitélio
normal) nas proximidades do tumor
Tabela 5: critérios de coloração de controlo interno
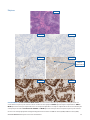
Caso 1 do controlo positivo interno: o carcinoma do endométrio não apresenta coloração de controlo interno nas proximidades das
células tumorais e, por isso, o carcinoma não pode ser avaliado. O Negative Reagent Control aceitável representado é NRC de ratinho
(mNRC).
Controlos positivos internos
As imagens representativas do controlo interno do VENTANA MMR RxDx Panel são apresentadas abaixo.
8 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio
H&E 40x mNRC 40x MLH1 40x

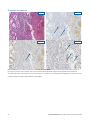
Caso 2 do controlo positivo interno: a coloração forte das células de controlo interno é apresentada nas proximidades do tumor
de carcinoma do endométrio de um caso com Estado de Perda de MLH1 e de um caso com Estado Intacto de MSH2. O Negative
Reagent Control aceitável é NRC de ratinho (mNRC).
MLH1 20x
Coloração das células de controlo interno Coloração das células de controlo interno
VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 9
H&E 20x mNRC 20x
MSH2 20x

Fluxo de trabalho de amostras
A realização de testes com VENTANA MMR RxDx Panel requer
várias secções de tecido em série de cada amostra de teste. É
necessária uma secção de cada para coloração com cada um dos
4 ensaios: VENTANA anti-MLH1 (M1) Mouse Monoclonal Primary
Antibody, VENTANA anti-PMS2 (A16-4) Mouse Monoclonal
Primary Antibody, VENTANA anti-MSH2 (G219-1129) Mouse
Monoclonal Primary Antibody e VENTANA anti-MSH6 (SP93)
Rabbit Monoclonal Primary Antibody. Além disso, são necessárias
secções de cada amostra de teste para coloração com H&E e com
anticorpo NRC correspondente à espécie do respetivo anticorpo
do VENTANA MMR RxDx Panel (mNRC ou rNRC).
Se a avaliação por H&E indicar que a amostra de paciente é
inadequada (por exemplo, se estiverem presentes menos de 50
células tumorais viáveis), deverá ser obtida uma nova amostra.
A repetição da coloração de uma amostra de um ensaio de
MMR RxDx específico dentro do painel (por exemplo, VENTANA
anti-MLH1 (M1) Mouse Monoclonal Primary Antibody) deve ser
realizada em lâminas não coradas se (1) a lâmina do caso corada
com o controlo de reagente negativo apropriado não apresentar
coloração aceitável, ou (2) se a lâmina do caso corada com
esse ensaio de MMR RxDx específico (por exemplo, VENTANA
anti-MLH1 (M1) Mouse Monoclonal Primary Antibody) não for
avaliável. Se qualquer uma das lâminas não for interpretável
devido a inexistência de coloração nas células do controlo positivo
interno, artefactos, efeitos de bordos, necrose, falta de tecido
ou qualquer outra razão, a lâmina não pode ser avaliada. Se os
controlos forem aceitáveis e as lâminas coradas com VENTANA
MMR RxDx Panel forem avaliáveis, as lâminas podem ser avaliadas
por um patologista com a devida formação, tal como é descrito no
Algoritmo de pontuação.
NOTA: o OptiView DAB IHC Detection Kit e o OptiView
Amplification Kit são os únicos reagentes de deteção
recomendados para utilização com o VENTANA MMR RxDx Panel.
10 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio

Fluxo da amostra
VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 11
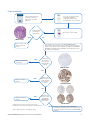
As secções com 4m de espessura
são montadas em lâminas
carregadas positivamente (são
necessárias 6 ou 7 secções em série).
Repita a coloração com
uma nova amostra de
paciente*
Não Sim
A lâmina de H&E
é aceitável (≥ 50
células viáveis)?
É corada uma secção em cada ensaio no VENTANA MMR RxDx Panel.
Adicionalmente, cada condição do ensaio é corada com controlo de reagente
negativo correspondente à espécie, Negative Control (Monoclonal) (mNRC) ou
Rabbit Monoclonal Negative Control Ig (rNRC), conforme aplicável no mesmo
processamento do instrumento.
O resultado de MMR (MLH1, PMS2, MSH2, MSH6) é
determinado por um patologista com a devida formação, de
acordo com o Algoritmo de pontuação do VENTANA MMR
RxDx Panel.
Não
Não
Não
Sim
Sim
Sim
A lâmina de
amostra corada
com o controlo de
reagente negativo é
aceitável?
Cada uma das
lâminas de amostra
coradas apresenta
controlos internos
aceitáveis?
As lâminas de
amostras coradas
com VENTANA
MMR RxDx Panel
são aceitáveis?
H&E do tumor
NRC do tumor
*A repetição pode ser feita no mesmo bloco do paciente
ou noutro bloco de tecido do mesmo paciente, conforme aplicável.
(Todas as imagens do tumor com ampliação de 20x)
Controlo interno
IHC do tumor
A amostra de tecido tumoral
é fixada em formol neutro
tamponado a 10% durante
6-72horas.
Uma secção é corada com H&E.
Repita o processamento
de coloração
Repita a coloração da
amostra*
Repita a coloração da
amostra*

12 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio
Imagens de referência
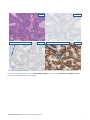
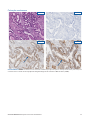
Caso proficiente 1: Estado Intacto de MLH1, PMS2, MSH2 e de MSH6 num carcinoma do endométrio que apresenta coloração
nuclear forte em células tumorais na presença de controlos internos corados de forma apropriada. Os Negative Reagent Controls
aceitáveis representados são NRC de ratinho (mNRC) e NRC de coelho (rNRC).
Casos proficientes
mNRC 20x
rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x
H&E 20x

VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 13
Caso proficiente 2: Estado Intacto de MLH1, PMS2, MSH2 e de MSH6 num carcinoma do endométrio que apresenta coloração
nuclear forte em células tumorais na presença de controlos internos corados de forma apropriada. Os Negative Reagent Controls
aceitáveis são NRC de ratinho (mNRC) e NRC de coelho (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

14 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio
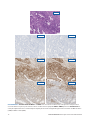
Caso deficiente 1: Estado de Perda de MLH1 e de PMS2 num carcinoma do endométrio que não apresenta coloração nuclear em
células tumorais na presença de controlos internos corados de forma apropriada. MSH2 e MSH6 apresentam Estado Intacto. A
coloração citoplasmática não é considerada para interpretação do estado. Os Negative Reagent Controls aceitáveis são NRC de ratinho
(mNRC) e NRC de coelho (rNRC).
Casos deficientes
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

VENTANA MMR RxDx Panel para o Carcinoma do Endométrio 15
Caso deficiente 2: Estado de Perda de MLH1 e de PMS2 num carcinoma do endométrio que não apresenta coloração nuclear
em células tumorais na presença de controlos internos corados de forma apropriada. MSH2 e MSH6 apresentam Estado Intacto. A
coloração citoplasmática não é considerada para interpretação do estado. Os Negative Reagent Controls aceitáveis são NRC de ratinho
(mNRC) e NRC de coelho (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x

16 VENTANA MMR RxDx Panel para o Carcinoma do Endométrio
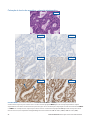
Caso deficiente 3: Estado de Perda de MSH2 e de MSH6 num carcinoma do endométrio que não apresenta coloração nuclear
em células tumorais na presença de controlos internos corados de forma apropriada. MLH1 e PMS2 apresentam Estado Intacto. A
coloração citoplasmática não é considerada para interpretação do estado. Os Negative Reagent Controls aceitáveis são NRC de ratinho
(mNRC) e NRC de coelho (rNRC).
H&E 20x
mNRC 20x rNRC 20x
MLH1 20x PMS2 20x
MSH2 20x MSH6 20x
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
A página está carregando ...
-
 1
1
-
 2
2
-
 3
3
-
 4
4
-
 5
5
-
 6
6
-
 7
7
-
 8
8
-
 9
9
-
 10
10
-
 11
11
-
 12
12
-
 13
13
-
 14
14
-
 15
15
-
 16
16
-
 17
17
-
 18
18
-
 19
19
-
 20
20
-
 21
21
-
 22
22
-
 23
23
-
 24
24
-
 25
25
-
 26
26
-
 27
27
-
 28
28
-
 29
29
-
 30
30
-
 31
31
-
 32
32
-
 33
33
-
 34
34
-
 35
35
-
 36
36
-
 37
37
-
 38
38
Roche BenchMark ULTRA Interpretation Guide
- Tipo
- Interpretation Guide
- Este manual também é adequado para
Artigos relacionados
-
Roche VENTANA PD-L1 (SP142) Assay Interpretation Guide
-
Roche VENTANA anti-ALK D5F3 Primary Antibody Manual do usuário
-
Roche uPath HER2 (4B5) image analysis for Breast Algorithm Manual do usuário
-
Roche uPath PD-L1 image analysis for NSCLC IVD Algorithm Manual do usuário
-
Roche VENTANA PD-L1 (SP263) Assay, Universal, CE IVD, Predictive, NSCLC Interpretation Guide






































